의약품 3D 프린팅 기술의 현재와 미래
목차
1. 3D 프린팅 의약품의 필요성과 현황
2. 3D 프린팅 기술의 특징과 분류에 따른 의약품 연구 동향
3. 3D 프린팅을 이용한 의약품 제형
4. 3D 프린팅 의약품의 미래 방향
5. 결론 및 제언
1. 3D 프린팅 의약품의 필요성과 현황
3D 프린팅 의약품 개발의 필요성
의약품 제조를 위한 3D 프린팅 기술
- 3D 프린팅 기술은 원하는 제품을 특정 소재를 활용하여 적층방식을 통해 현장에서 실시간으로 제조할 수 있는 기술임.
- 3D 프린팅 기술은 4차 산업혁명을 주도하는 핵심 기술분야 중 하나로서 최근 장비의 대중화와 함께 그 활용이 크게 증가 하고 있음.
- 의약품 중 가장 널리 사용되는 경구용 정제(tablet) 및 캡슐제(capsule) 등은 현재 대부분 조형가공에 의해 제조되며 값싸 고 빠르게 대량 생산이 가능한 장점이 있으나, 환자들의 다양한 특성에 맞는 의약품을 소량으로 생산이 가능한 맞춤형 소 량 생산 방식에는 적합하지 않음.
- 3D 프린팅은 다양한 소재를 가지고 다양한 형태의 구조물을 신속하게 소량 생산할 수 있는 방식으로 개인 맞춤형 의약품 의 제조에 최적화된 생산방식으로 평가됨. 개인 맞춤형 의약품
- 기존 의약품의 개발과 생산은 모든 환자를 대상으로 설계되는 형태로서 환자 개개인의 개별 특성을 반영한 환자별 최적화 는 할 수 없음 [1].
- 현재 개인의 유전적 다형 (genetic polymorphism)으로 인해 다양한 치료의 실패와 부작용 사례가 보고되어 있음 [2].
- 2008년 미국에서 전체 처방된 의약품 중 거의 절반에 가까운 3,000억 달러 규모의 의약품이 대상환자에게 의료 효과를 나 타내지 못한 것으로 조사되어 있으며, 미국에서 의약품 부작용으로 사망하는 환자의 수는 연평균 137,000명에 달하는 상 황임 [3].
- 이는 주로 개인별 환자의 유전적 특성을 고려하지 못한 것이 주요 원인중의 하나로 인식되고 있음.
- 따라서 정밀한 환자 맞춤 의약품 개발을 통해 치료효과의 극대화와 부작용의 최소화하려는 시도가 필요함. 3D 프린팅 기술을 이용한 의약품의 개발
- 2015년 8월 최초로 3D 프린팅으로 제조한 의약품인 Spritam이 미국 FDA에서 승인을 받음.
- Spritam은 미국 Aprecia pharmaceutical사에 의해 개발되었으며 뇌전증 치료제인 levetiracetam 성분을 포함하고 있고 빠른 붕해를 위해 기존의 정제 제조공정 대신 3D 잉크젯 프린팅 기술인 Zipdose 기술을 이용하여 제조한 다공성 구 조의 속붕해성 제형임.
- Spritam의 출시로 인해 실제로 의약품의 제조가 3D 프린팅 공정으로 생산이 가능함을 확인하였으며, 이는 100년 이상 유지되어 온 기존의 의약품 생산 방식에 대한 새로운 접근법을 제시함.
- 하지만 Spritam의 2018년 매출은 22억에 불과하며 현재는 생산이 중단된 상태로서 시장에서의 파급력은 미약함.
- 이는 기존의 제형과 차별화되는 장점 없이 단지 3D프린팅 기술을 적용하여 의약품을 생산하는 것만으로는 시장에서 성공 할 수 없다는 현실을 보여줌.
- 따라서 미래 3D 프린팅 기술을 활용한 제형이 성공하기 위해서는 다양한 제품을 소량 생산할 수 있는 다품종 소량생산이 라는 3D 프린팅 고유의 장점 이외의 기존의 제형과는 차별화되는 새로운 장점을 갖는 제형을 개발하려는 접근이 필요함.
- 현재 3D 프린팅 기술을 이용한 다양한 형태의 의약품 개발이 시도되고 있으며 그 내용을“3. 3D 프린팅을 이용한 의약품 제형”에 요약하였음.
3D 프린팅 의약품의 장점
제형 설계 능력 향상
- 3D 프린팅은 여러 부분으로 이루어진 조립품을 하나의 공정으로 제조할 수 있으며 유기적인 형태로 제작이 가능함.
- 즉 여러 부분으로 이루어진 의약품을 한 공정으로 통합하여 인쇄할 수 있음을 의미함.
복잡한 구조의 의약품 제조
- 3D 프린팅은 복잡한 구조를 가진 의약품을 생산하기 어려운 기존 제조법에 비하여 복잡한 구조물을 제조할 수 있음.
- 단순한 형태의 기존 제형(정제, 캡슐제 등)과 다르게 더욱 복잡한 형태의 제형 설계가 가능하며 이를 통하여 약물의 방출조 절이 가능함.
사용자 특성 맞춤형 의약품 제조
- 특정 환자와 사용자의 개별 요구 사항에 따라서 의약품을 맞춤화할 수 있음.
주문형 제작 및 다품종 소량생산
- 필요에 따라 의약품 제조가 신속하게 이루어질 수 있고 소량으로 생산이 가능함.
재료 효율성 증가
- 제조 방법의 특성상 의약품 생산에 필요한 원료의 양과 제조에 사용된 원료의 양이 거의 일치함.
- 궁극적으로 수요에 따른 생산을 지향하며 과잉 생산으로 인한 재고 관리의 어려움을 극복할 수 있음.
자원의 효율성 증가
- 의약품 제조용 장비를 위해 더 적은 자원을 사용하고 낮은 숙련도의 인력으로도 제조가 가능함.
- 기존 제조법에 비해 더 적은 생산도구를 사용함.
개발 비용과 위험 감소
- 개념에서 제조까지의 개발 시간이 최소화되기 때문에 상업적 이익과 경쟁력 향상은 비용 및 위험 감소의 형태로 나타남.
- 3D 프린팅을 통한 제조는 생산 단가 상승이 발생하므로 상승된 단가 대비 유용성을 평가할 필요가 있음.
제조 장소의 다변화
- 프린팅 할 의약품을 디지털 방식으로 전송하여 소비자와 가까운 장소나 가정에서 인쇄할 수 있으므로 운송 요건과 운송 의 존도가 줄어듦.
- 운송수단에 의해 발생하는 배기가스의 배출량 감소로 인하여 친환경적임.
3D 프린팅의 공정 분류 (Process categories)
제품의 제조 방법은 크게 적층가공, 절삭가공 그리고 조형가공으로 나눌 수 있으며 3D 프린팅은 이 중 적층가공으로 분류됨 (그림 1).

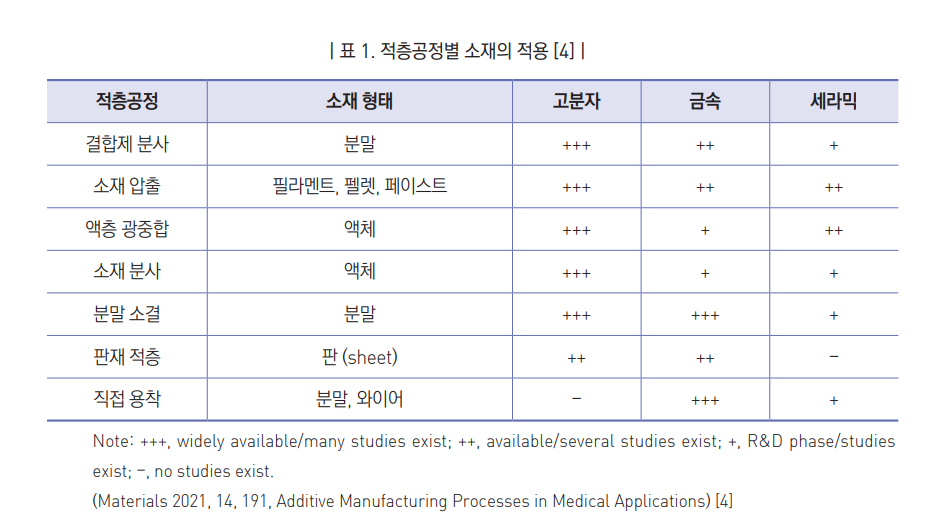
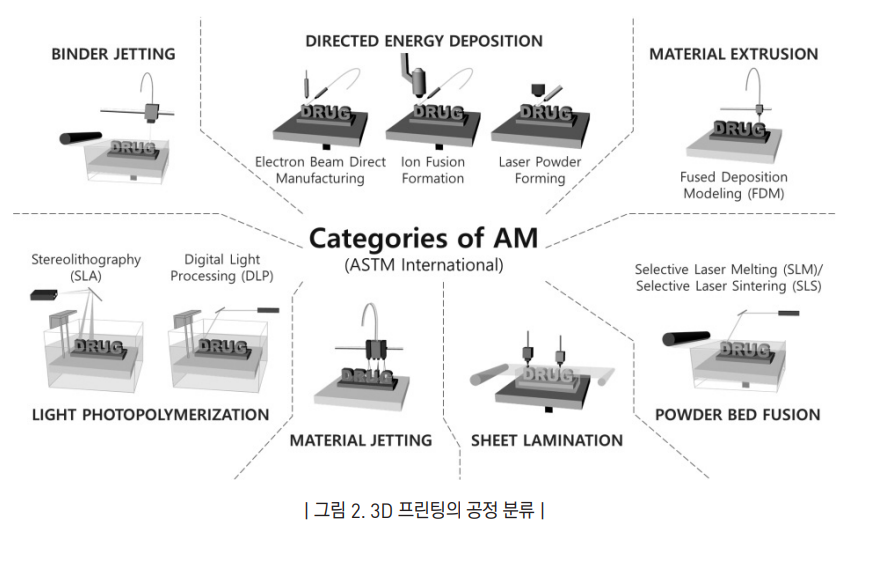
국제표준개발기관 ASTM International에서는 적층가공의 공정을1) 1) 결합제 분사 (binder jetting) 2) , 2) 소재 압출 (material extrusion), 3) 액층 광중합 (vat photopolymerization), 4) 소재 분사 (material jetting), 5) 분말 소결 (powder bed fusion), 6) 판재 적층 (sheet lamination), 그리고 7) 직접 용착 (directed energy deposition)의 7가지로 분류하고 있음 (그림 2).
최근에 개발되는 다양한 3D 프린팅 장비들은 위의 분류된 공정에 해당하거나 이들을 서로 융합한 형태로 존재함.
ASTM International에서 분류한 적층가공의 공정을 간단하게 설명하면 다음과 같으며 이중 판재 적층과 직접 용착을 제외 한 나머지 공정을 활용한 의약품 연구가 보고되어 있음.
- 결합제 분사 (binder jetting): 분말 소재를 굳히기 위해 액상 결합제가 선택적으로 분사되는 방식의 적층 가공 공정으로 분말로 되어 있는 의약품 원료에 대하여 적용이 가능함. 이 방식은 FDA에서 최초로 승인된 의약품인 Spritam을 제조하 는 방식임.
- 소재 압출 (material extrusion): 장비 헤드에 장착된 노즐 또는 구멍을 통하여 소재를 선택적으로 압출시키는 방식의 적 층 가공 공정으로 FDM (Fused Deposition Modeling) 혹은 FFF (Fused Filament Fabrication) 방식으로 알려져 있음. 의약품을 주로 필라멘트의 형태로 가공해서 적용하며 바이오프린팅에 주로 사용하는 주사기를 사용한 적층방식이 포함됨.
- 액층 광중합 (vat photopolymerization): 액상 광경화성 수지가 레이저 혹은 자외선에 의한 광중합 (light-activated polymerization) 반응에 의해 선택적으로 경화되는 방식의 적층 가공 공정으로 SLA (Stereolithography)와 DLP (Digital Light Processing) 방식의 3D 프린터가 이 방식에 포함됨. 소재에 의약품을 포함해서 3D 프린팅할 경우 레이 저나 자외선에 의한 의약품의 품질변화가 우려될 수 있으며 광경화에 사용되는 물질에 대한 독성 우려가 존재함.
- 소재 분사 (material jetting): 소재의 입자를 선택적으로 분사하여 적층 제작하는 공정으로 2D 프린팅 공정 중 잉크젯 프 린팅 공정과 유사함. 소재를 분사 후 경화를 위해 주로 자외선을 사용하며 액체형태의 열경화성 고분자나 왁스류를 소재로 사용함. 의약품에 적용되는 방법은 주로 미리 제조된 필름이나 정제에 의약품 용액을 분사하는 방식으로 적용됨.
- 분말 소결 (powder bed fusion): 분말 구역을 열 에너지를 사용하여 선택적으로 녹이는 방식의 적층 가공 공정으로 SLS (Selective Laser Sintering) 방식이 포함됨. 약물을 포함한 고분자에 레이저를 가해서 고분자를 소결시키는 방식으로 의약품을 제조할 수 있음. 적층을 위해 고에너지가 집적되므로 의약품의 안정성에 영향을 미칠 우려가 있음.
- 판재 적층 (sheet lamination): 판 형태의 소재를 원하는 형태로 잘라서 적층시켜 출력물을 제작하는 방식의 적층 가공 공정으로 LOM (Laminated Object Manufacturing) 방식이 포함됨. 필름형태의 의약품에 적용이 가능할 것으로 예상 되나 아직까지 의약품에 적용한 사례는 보고되지 않음.
- 직접 용착 (directed energy deposition): 소재에 집중적으로 열 에너지를 조사하여 녹이고 결합시키는 방식의 적층 가 공 공정으로 주로 메탈 3D 프린팅에 광범위하게 적용되는 공정임. 아직까지 의약품에 적용한 사례는 보고되지 않음.
2. 3D 프린팅 기술의 특징과 분류에 따른 의약품 연구 동향
결합제 분사(binder jetting)
기본원리 및 특징
- 결합제 분사 방식의 기본원리는 액체로 되어 있는 결합제를 분말층에 분사하여 단면층을 고형화 시키는 것임
- 각 층은 기존의 인쇄용 프린터가 잉크를 종이에 인쇄하는 것과 거의 동일한 방식으로 인쇄됨.
- 각 단면이 완료되면 빌드 플랫폼이 아래로 이동하고 새로운 분말들이 그 위에 가해진 후에 자동 롤러가 평평하게 얇은 층 을 형성시키고 다시 결합제가 분사되는 공정을 반복하게 됨.
- 결합제 분사 방식은 각 층의 차이가 보이지 않는 특징이 있으며 프린팅 공간을 넓게 확장하면 대량 생산이 가능함.
- FDA에서 최초로 승인된 의약품 (Spritam)의 제조에 사용된 방식임. - 결합제 분사방식의 특징은 사용하고자 하는 약물의 분말입자 크기나 첨가제들의 입자크기에 따라 한 층의 높이가 영향을 받게 됨.
- 결합제 분사 방식으로 의약품을 제조할 경우 사용된 용매인 물이나 에탄올 등이 제거될 수 있도록 건조하는 후처리 과정이 요구되기도 함.
의약품 제조에 있어 장점과 단점
- 장점: ①가장 큰 장점은 기존 의약품에 사용하던 소재들을 그대로 사용 가능하다는 것임. ②정제나 캡슐제 등에 사용하던 첨가 제 분말층에 결합제로 사용하는 첨가제 용액을 분사해서 3D 프린팅 의약품을 제조할 수 있음. ③결합제 분사방식의 다른 장점은 실온에서 분말들의 결합이 이루어진다는 것임. ④다른 방식들(FDM, SLS 등)과 다르게 열이 가해지면서 발생하는 비틀림 등의 형태 변화가 발생하지 않음. ⑤기존 정제 제조 공정에 비해서 속도가 느리긴 하지만 대량 생산이 가능함. ⑥결 합제가 적용되지 않고 공정 중 제거된 분말은 재사용이 가능함. ⑦지지체(supporter)가 따로 필요하지 않음. 즉 공정 중 결합제에 의해 굳어지지 않은 주변 분말은 지지체로 작용함.(SLS와 유사). 이는 일반적으로 지지체 구조가 없을 경우 휘어 짐이 발생할 수 있는 구조를 제조할 때 유리하게 작용할 수 있음. ⑧결합제 분사 방식으로 제조할 경우 제조되는 출력물이 빌드 플랫폼의 바닥에 부착되지 않아도 되므로 제조되는 빌드 플랫폼 전체 공간을 활용할 수 있음. ⑨결합제 분사방식으로 제조하려고 하면 빌드 플랫폼의 전체 공간을 효과적으로 채우는 방법을 고려하는 것이 매우 중요함.
- 단점: ①결합제 분사 공정으로 생성된 의약품은 사용되는 재료와 미립자 간의 접착력이 낮을 수 있어서 다른 적층 제조 기술과 다르게 충분한 기계적 강도를 갖지 못할 수도 있음. ②공정 후 남아있는 과잉의 분말은 압축 공기를 사용하여 완전히 제거 해야 함. ③복잡한 구조의 의약품을 제조하는데 한계가 있음.
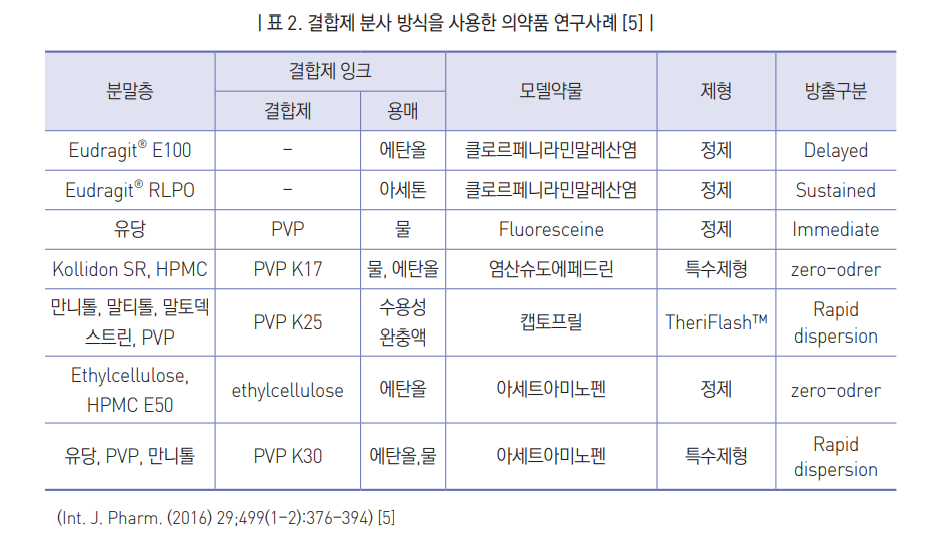
의약품 제조에 적용된 사례
- FDA에서 최초로 승인된 의약품인 Spritam®의 제조에 사용된 방식임.
- 기존 의약품에 사용 가능한 소재를 사용할 수 있으므로 많은 사례가 보고됨.
소재 압출(material extrusion)
기본원리 및 특징
- 소재 압출 방식은 프린팅하고자 하는 소재를 노즐을 통해 압출하면서 원하는 형상으로 적층하는 방식으로 우리가 흔히 알 고 있는 가장 대중적인 3D 프린팅 방식인 FDM 방식이 여기에 속하며 상용화된 3D 바이오프린터는 대부분 소재 압출 기 반의 프린팅 공정을 사용함.
FDM (Fused Deposition Modeling)/FFF (Fused Filament Fabrication)
- FDM은 일반적인 소재 압출공정을 의미하며 스트라타시스사의 상표로 등록되어 있기 때문에 상표권 관련 분쟁을 사전에 막기 위해 오픈소스 분야에서는 같은 방식을 FFF(Fused Filament Fabrication)로 표기함.
- 이 방식은 일종의 자동화시킨 글루건과 유사한 방식으로 열가소성 물질을 필라멘트 형태로 만들고 노즐을 통과시켜 용융 하여 원하는 형태를 만드는데 필요한 부분에 용융된 물질을 밀어내어 응고시키면서 아래부터 쌓아올려 3D 프린팅 하는 방 식임.
- FDM은 일반적인 소재 압출공정을 의미하며 스트라타시스사의 상표로 등록되어 있기 때문에 상표권 관련 분쟁을 사전에 막기 위해 오픈소스 분야에서는 같은 방식을 FFF(Fused Filament Fabrication)로 표기함.
- 이 방식은 일종의 자동화시킨 글루건과 유사한 방식으로 열가소성 물질을 필라멘트 형태로 만들고 노즐을 통과시켜 용융 하여 원하는 형태를 만드는데 필요한 부분에 용융된 물질을 밀어내어 응고시키면서 아래부터 쌓아올려 3D 프린팅 하는 방 식임.
- 노즐의 크기 및 용융되어 밀어내는 속도와 힘에 따라서 층의 크기와 디테일이 결정됨. 노즐로 물질을 녹여 밀어내기 위해 선 노즐을 가열하여 온도를 높이는 과정이 필요하며 용융되어 나온 필라멘트는 상온에서 굳으며 형태를 갖추게 됨.
- 특징으로는 출력물이 강도가 강하고 습도에 강해 내구성이 뛰어남.
- 다른 프린터에 비해 구조가 단순하고 사용법이 간단해 가격과 유지보수 비용이 낮은 편이며 다양한 소재 적용이 가능하고 기기 컨트롤의 정밀도에 따라 모델의 표면 조도 개선이 가능함.
- 단점으로는 표면이 거칠고 제작 속도가 다른 방식에 비해 느림.
Pressure Assisted Microsyringe (PAM)
- PAM은 공기압 또는 기계적 힘을 이용해 주사기 안에 있는 출력물을 필라멘트 형태로 압출하여 3D 구조체를 제조함.
- 상온에서 프린팅이 가능하므로 바이오프린팅에 많이 적용되며 하이드로겔 형태의 내용물을 출력할 수 있음.
- PAM은 압축공기, 피스톤이나 스크류에 의한 기계적 혹은 솔레노이드 기반 시스템으로 작동함.
- 압축공기를 사용한 압축 베이스 시스템과 피스톤이나 스크류 작동 형태를 활용한 기계적 마이크로 압출 시스템이 있음.
- 피스톤 형태가 일반적으로 노즐을 통해 소재의 흐름을 직접 조절할 수 있고 스크류 시스템은 고점도의 소재를 압출하는 데 좀 더 유용함.
- 프린트된 3D 구조체는 프린팅 후 형태를 유지하고 구조체의 기계적 강도를 높이기 위해 광경화 또는 화학적 가교로 추가 적인 처리를 해야 함.
- 사용 가능한 소재는 필라멘트 형태로 출력이 가능한 물질이 적합하며 온도에 반응하여 젤화되는 collagen, Matrigel들과 광경화되는 gelatin methacryloyl, collagen methacryloyl, hyualuronic methacrylate들과 칼슘이온으로 젤화되 는 alginate 등이 있음.
- PAM의 가장 큰 단점은 낮은 해상도(200-1000 µm)로 정밀하게 패턴화 및 조직화하기 어려움.
- 액체나 졸겔 상태의 바이오잉크가 원통형 필라멘트의 형태로 압출되기 위해서는 표면장력에 의한 액적 형성을 위해 전단 감소특성(shear thinning properties)을 가져야 함.
- PAM에 금속 주사기를 사용해 온도를 고온으로 높여 적용할 경우 FDM 방식과 유사하게 출력이 가능함.
의약품 제조에 있어 장점과 단점
- 장점: ①FDM 방식은 필라멘트 제조를 위해 제약산업의 기존 기술인 고온압출용융법 (hot melt extrusion)을 응용할 수 있으 므로 의약품 제형 연구가 가장 많이 진행되고 있는 기술임. ②약물을 포함한 필라멘트 제조를 위해서는 사용되는 고분자 물질과 약물의 최적화 비율을 찾아야 하며 유연성을 위해 가소제가 첨가될 수 있음. ③고온에서 분해가 되는 약물을 적용 하기 어려운 단점이 있고 약물의 특성상 필라멘트 형성이 어려운 경우 많은 양의 고분자가 필요해 고용량의 제형을 제조하 는데 어려움이 있음. ④FDM 방식은 붕해제가 포함되기 어렵기 때문에 빠른 약물방출이 필요한 제형의 경우 적절한 디자인 설계 혹은 출력방법 (infill, shell thickness 조절)에 의한 붕해속도 조절이 필요함. 프린팅 공정 중에 고온이 가해지므 로 열에 의한 비틀림이나 팽창/수축이 발생할 수 있고 여러 약물을 동시에 하나의 제형으로 적용해 프린팅할 경우 열적 특 성을 확인할 필요가 있음. ⑤작은 직경의 노즐을 사용해 출력물의 표면 거칠기를 조절할 수 있으나 직경이 작은 노즐을 사 용할 경우 상대적으로 출력속도가 더 느려져 출력물의 표면 품질과 생산성이 반비례하는 단점이 있음.
- 단점: ①상온에서 프린팅하는 PAM 방식은 해상도가 낮아 크기가 작은 경구용 의약품을 제조하는데 어려움이 있으며 FDM과 유사하게 고온에서 프린팅하는 금속주사기를 사용한 PAM 방식은 용융된 약물과 고분자물질의 점도가 상대적으로 높으 므로 프린팅에 높은 압력이 필요함. ②또한 FDM과 다르게 거의 액체상태로 용융된 고온의 액체가 상온으로 프린팅되면서 빠르게 응고되어 출력조건을 최적화하는데 어려움이 존재함. ③고온 PAM의 경우도 사용되는 소재들의 열적 변형에 대한 특성을 이해하는 것이 중요함.
액층 광중합(vat photopolymerization)
기본원리 및 특징
- 액층 광중합 (vat photopolymerization)은 액상 광경화성 수지에 빛을 조사하여 경화시켜 한층씩 적층하는 방식으로 SLA (Stereolithography)와 DLP (Digital Light Processing) 방식이 포함됨.
- 액상의 광경화수지는 UV 레이저와 만나면 고체로 변하는데, 광경화 작용을 이용해 형상의 단면을 생성하고, 수조 내에 잠 겨있는 빌드 플랫폼이 단계적으로 하강 혹은 상승하면서 연속적으로 3차원 형상을 제조함.
- 액층 광중합 방식은 복잡한 형상의 부품을 만드는 데 적합하며 높은 치수 정확도와 표면 조도를 기대할 수 있음.
- 투명하거나 유연한 재료 혹은 생체 적합성 수지 등도 출력이 가능함.
SLA (Stereolithography)와 DLP (Digital Light Processing)
- SLA는 액체의 광경화성 수지가 담긴 수조에 레이저빔을 조사하여 필요한 부분을 경화시키고 한 층이 완료되면 수조가 한 층 하강(또는 상승)하고 다시 한층을 경화시키는 과정을 반복하여 구조체를 완성함.
- DLP는 DLP 프로젝터의 UV빔을 광원으로 하는 점을 제외하면 SLA 방식과 유사함. SLA는 레이저가 패턴을 따라 이동하 면서 수지를 경화시키지만 DLP는 한 면을 통째로 경화시키기 때문에 SLA보다 속도가 빠른 장점이 있음.
액층 광중합을 이용한 의약품 제조
- SLA를 이용한 의약품 제조의 예로는 Poly(ethylene glycol) diacrylate (PEGDA)를 단량체로 사용하고 diphenyl(2,4,6-trimethylbenzoyl)phosphine oxide를 광개시제로 사용하였으며 아세트아미노펜과 4-아미노살리실 산을 모델약물로 하여 PEG300을 인쇄용액에 첨가하여 정제를 제조하였음.
- 인쇄된 정제에서 아세트아미노펜과 4-아미노살리실산의 로딩은 각각 5.69%와 5.40%이었음 [6].
- 이 연구와 같은 광경화성 수지를 이용해 아세트아미노펜, 카페인, 나프록센, 클로람페니콜, 프레드니솔론 및 아스피린을 포함한 제형을 제조한 연구가 보고되었음 [7, 8].
- DLP를 이용한 의약품 제조의 예로는 SLA에서 사용된 광경화성 수지를 이용해 리보플라빈과 이부프로펜을 포함한 제형 이 보고되어 있음 [9].
소재 분사(material jetting)
기본원리 및 특징
- 소재 분사는 액상의 광경화성 수지를 노즐에서 분사하고 광에너지를 이용해 경화시켜 적층하는 방식으로 2차원 잉크젯 프 린터와 유사한 방식으로 구조체를 제작함.
- 소재 분사는 액상 수지를 30 - 60℃로 가열하여 최적의 인쇄 점도로 조정한 후 인쇄 헤드가 빌드 플랫폼 위로 이동하며 수 백 개의 작은 광중합체 액적이 분사됨.
- 인쇄 헤드에 부착된 UV 광원은 적층된 소재를 응고시키고 구조체의 첫 번째 층을 제조함.
- 한 층이 완료되면 빌드 플랫폼은 한 층 높이 아래로 이동하고 전체 부품이 완료될 때까지 프로세스가 반복됨. - 이 방식은 한 공정에 여러 소재를 사용할 수 있으며 제작 중에 소재를 변경할 수 있음.
- 소재 분사 방식은 병렬 구조로 배열된 재료 저장 장치에서 소재를 각각의 프린터 헤드로 공급하기 때문에 여러 가지 재료 를 동시에 사용할 수 있음.
- 소재는 점성이 강한 성질과 액적 형성 능력이 중요하며 점성이 주요 결정 요인임.
- 소재는 열 또는 압전 액추에이터로부터 노즐 압력 변화에 의해 분사되고 이는 잉크젯 프린팅의 원리와 유사함.
- 압전 액추에이터가 더 넓은 범위의 재료 사용이 가능함. 높은 정밀도와 여러 소재를 동시에 사용할 수 있는 장점이 있지만 사용 가능한 소재가 제한되어 있음.
의약품 제조에 있어 장점과 단점
- 약물을 광경화 액상수지와 혼합해 소재 분사 방식을 적용할 경우 약물로 인해 구조체가 경화되는 속도가 영향을 받지 않아 야 하고 약물이 광경화성 수지와 반응성이 없어야 하며 광에너지에 의한 약물의 분해가 없어야 함.
- 이와 같은 제약조건으로 인해 소재 분사에 적용되는 의약품들은 분사하면서 직접 구조체를 형성하는 경우 보다는 필름에 약물용액을 분사해 응용하는 경우가 주로 보고되어 있음.
- 예를 들어, Buanz et al.은 열전사 잉크젯 프린트 헤드를 기반으로 황산살부타몰 용액을 감자전분으로 만든 다공성 구강 필름 표면에 분사시켜 필름제형을 제조하였으며, 자궁경부암 치료를 위해 파클리탁셀-시클로덱스트린 포접 복합체와 시 도포비어(cidofovir)-PCL 나노입자를 생체 접착 필름에 인쇄하고 장기 방출 거동을 연구한 보고가 있음 [10, 11].
분말 소결(powder bed fusion)
기본원리 및 특징
- 분말 소결 방법의 하나인 선택적 레이저 소결(Selective Laser Sintering; SLS)의 제조 공정은 분말통 및 제작 부위가 고분자의 용해 온도에 가깝게 가열되며, 블레이드에 의해 빌드 플랫폼에 얇은 분말층을 도포함.
- 그 후 레이저에 의해 고분자 분말의 입자가 선택적으로 소결됨. 한 층이 완료되면 빌드 플랫폼이 아래로 이동하고 블레이 드가 표면에 다시 분말층을 도포함. - 그 후 전체 부품이 완료될 때까지 프로세스가 반복됨.
- SLS의 주요 장점은 소결되지 않은 분말이 지지체로 작용하므로 지지 구조가 필요하지 않음.
- SLS는 지정된 높이의 분말통에서 인쇄되는 부품의 수와 관계없이 인쇄하는데 거의 같은 시간이 소요되므로 빌드 볼륨을 충분히 활용하는 것이 필요함.
- 일반적으로 SLS 인쇄는 다공성을 갖게 되며 특유의 거친 표면 마감을 갖게됨. 출력된 구조체는 수축과 비틀림에 민감하므 로 관련된 특성을 파악할 필요가 있음.
분말 소결 방식을 이용한 의약품 제조
- 고출력 레이저에 의한 의약품의 안정성 여부가 중요하며 적절하게 소결시킬 수 있는 특성의 고분자 물질 선정이 필요함.
- 다공성을 활용한 약물방출조절의 가능성이 존재하지만 구조체의 거친 표면의 특성으로 인해 외관이 우수하지 못한 단점이 있음.
분말 소결 방식으로 제조된 의약품 연구 사례
- 두 종류의 생체분해성 고분자인 Polycaprolactone (PCL)과 Polylactic Acid (PLLA)에 대해서 레이저 출력, 레이저 스 캔 속도 및 부품 베드 온도가 다공성 미세 구조 형성에 미치는 영향을 확인하여 약물전달장치로 사용할 수 있는 다공성 고 분자 매트릭스 정제를 제조함 [12].

3. 3D 프린팅을 이용한 의약품 제형
3D 프린팅 기술을 이용한 경구용 방출조절 제형
3D 프린팅 기술을 이용한 속붕해정 (Rapid dissolving tablet, RDT))의 제조
- 속붕해정은 구강내의 타액과의 접촉으로 인해 빠른 시간 내에 구강에서 붕해가 이루어져 액체 상태로 흡수가 되는 정제로 서 신속하게 물을 흡수하여 빠르게 붕해할 수 있도록 제조되어야 함.
- 정제를 삼키기 힘든 환자들이 (소아나 노인 또는 뇌전증 질환자) 속붕해정을 통해 효과적으로 약물을 복용할 수 있음. - 속붕해정은 동결건조, 주형법, 타정법, 분무건조법, 소결법 등으로 제조되며 가장 일반적인 제조방식인 타정법의 경우 정 제의 적절한 경도와 정제 내부의 적절한 공극 사이의 균형을 유지하는 최적의 타정압을 설정하는 것이 매우 중요함.
- 3D 프린팅 기술을 이용하여 만든 Rapid dissolving tablet의 대표적인 사례로는 세계 최초로 미국 FDA의 승인을 받은 뇌전증 치료제인 Spritam이 있음.
- 아래의 표 3에 3D 프린팅 기술을 이용하여 제조한 속붕해정의 사례를 요약하였음.


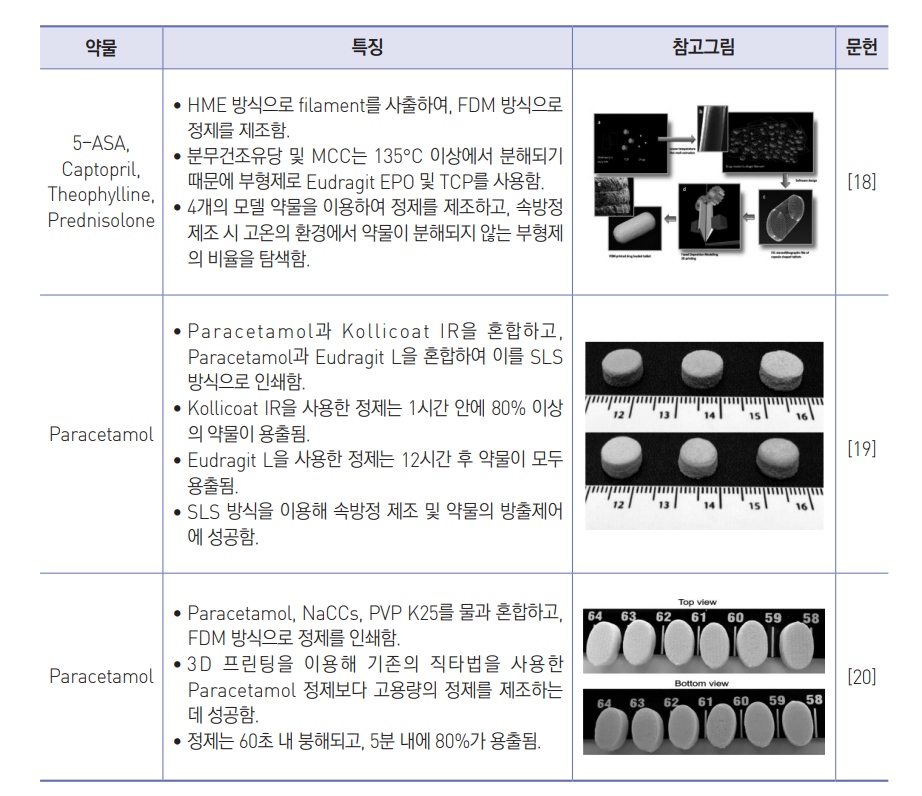
3D 프린팅 기술을 이용한 속방정 (Immediate release tablet, IR)의 제조
- 3D 프린팅 기술을 이용하여 다양한 함량과 내부구조를 갖는 속방정 (Immediate release tablet, IR)을 제조한 결과가 보고되어 있으며 그 내용을 표 4에 요약하였음.

3D 프린팅 기술을 이용한 서방정 (Extended release tablet)의 제조
- 서방정은 약물의 위장관에서의 방출속도를 변화시켜 약물의 흡수속도를 조절하고 이를 통해 약물의 혈중농도 지속시간을 변화시킬 수 있음.
- 개인의 치료학적 상황에 따라 개인별 약물의 방출속도 조절이 필요할 수 있지만 현재의 제형개발 방식으로는 개인별 맞춤 약물의 생산은 어려움.
- 현재 3D 프린팅 기술을 이용하여 방출속도가 다른 경구용 정제를 제조하는 연구가 진행 중임.
- 대부분 정제 형태 혹은 내부의 충전 (infill) 정도를 변경하거나, 정제를 인쇄하는 부형제의 조성을 변경하여 방출속도를 조 절하는 연구가 이루어지고 있으며 다양한 사례를 표 5에 요약하였음.



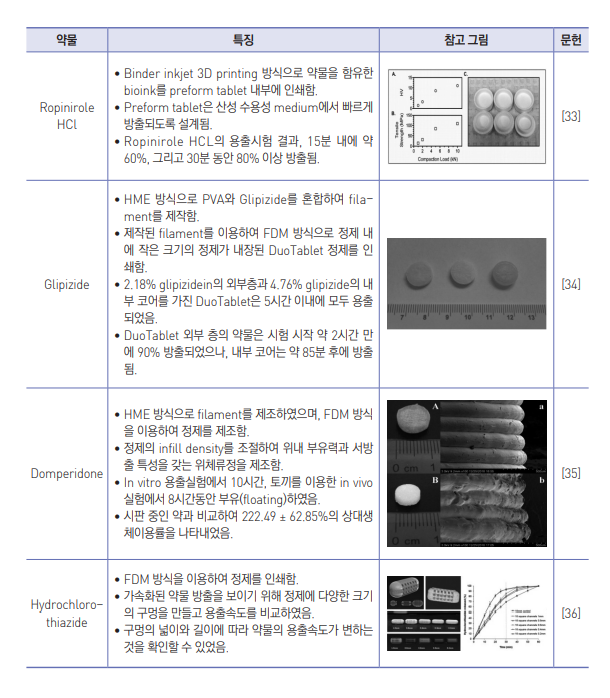
3D 프린팅 기술을 이용한 지연방출 정제 (Delayed release tablet)의 제조
- 지연방출 시스템은 주로 위에서의 약물의 방출을 억제하고 장에 도달할 때까지 지연시키는 장용시스템이 일반적임.
- 이러한 장용시스템은 약물이 위내 낮은 pH 환경에서 불안정하거나, 약물이 위점막에 자극을 주는 경우에 사용함.
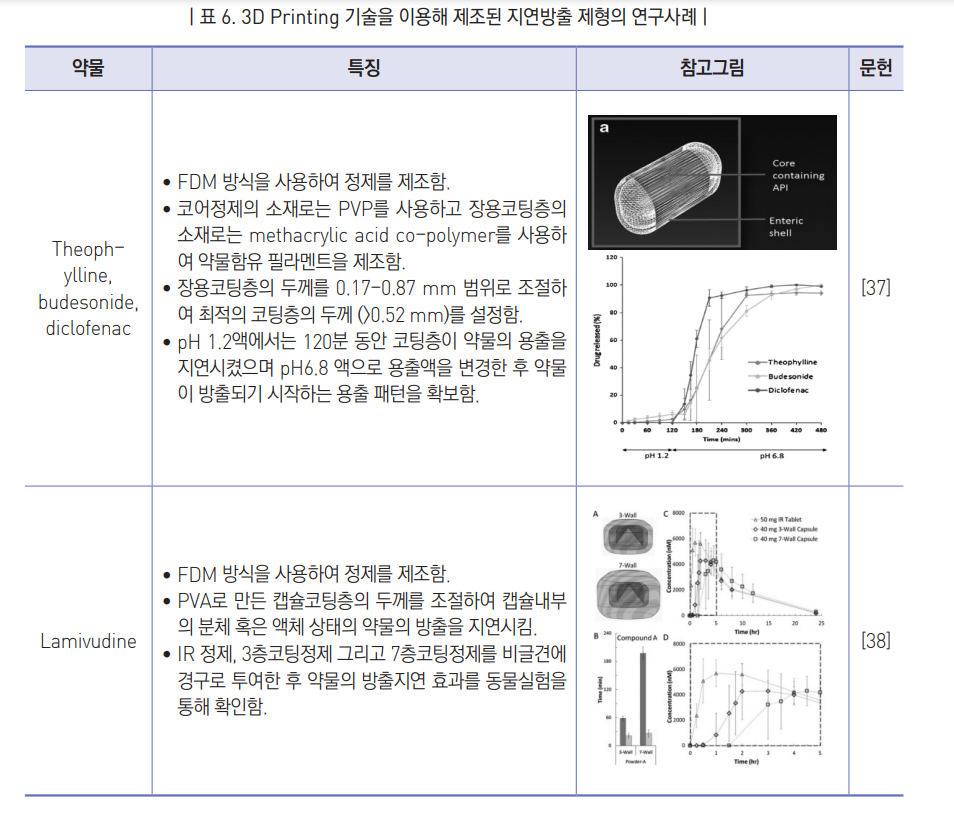
- 장용정의 제조는 대부분 원료의약품이 탑재된 코어층의 제조와 코어층을 위에서 보호되도록 하는 장용코팅의 두 과정으로 이루어지며 3D 프린팅 제형 또한 서로 다른 물질로 코어층과 코팅등을 인쇄하는 방식으로 제조됨 [35].
- 기타 코팅층의 두께를 조절하여 약물의 지연방출속도를 조절하는 경우도 있음.
- 표 6에 3D 프린팅 기술을 이용하여 제조한 지연방출 정제의 제조 사례를 요약하였음.
3D 프린팅 기술을 이용한 다제복합제 (Polypill)의 제조
- Polypill은 다수의 약물을 하나의 정제 또는 캡슐 형태로 제조하는 제형이며, 다양한 개인의 치료학적 상황에 따라 약물의 종류, 용량 그리고 방출패턴의 설정이 가능함.
- Polypill은 다양한 약물을 한 개의 정제에 담을 수 있는 기술로서 환자가 여러개의 정제를 복용해야 하는 불편함을 줄여 개 인의 복약순응도를 높일 수 있는 기술임.
- 3D 프린팅 기술을 이용하여 제조한 다양한 polypill의 사례를 표 7에 요약하였음.


3D 프린팅 기술을 이용하여 만든 방출제어 용기
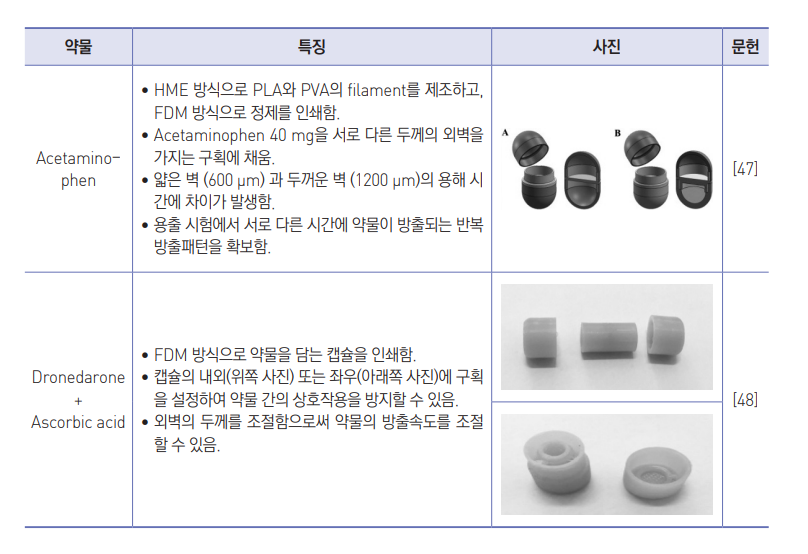
- 방출제어 기능성 용기는 약물의 종류 상관없이 용기 자체가 방출조절 기능을 갖기 때문에 용기와 용기 내부에 충전되는 다 양한 약물과의 조합을 통해 다양한 개인 맞춤형 의약물을 제조할 수 있는 특징을 가짐.
- 3D 프린팅 기술은 다양한 형태의 방출제어 기능성 용기를 적은 비용으로 신속하게 제조할 수 있는 기술로서 방출제어 기 능성 용기 제작과 개발에 필수적인 기술임.
- 현재 3D 프린팅 기술을 이용한 다양한 방출제어 용기 개발연구가 진행중이며 그 사례를 표 8에 요약하였음.

비경구용 제형에 있어서의 3D 프린팅 기술의 도입
3D 프린팅 기술을 이용한 경피투여시스템의 제조
- 경피로 투여되는 제형은 경구투여 다음으로 활발하게 연구가 이루어지고 있는 분야 중 하나로서, 3D 프린팅 기술을 활용 한 경피투여시스템 연구 역시 활발하게 연구가 진행중임.프린팅 기술을 이용한 경피투여시스템의 제조
- 경피로 투여되는 제형은 경구투여 다음으로 활발하게 연구가 이루어지고 있는 분야 중 하나로서, 3D 프린팅 기술을 활용 한 경피투여시스템 연구 역시 활발하게 연구가 진행중임.
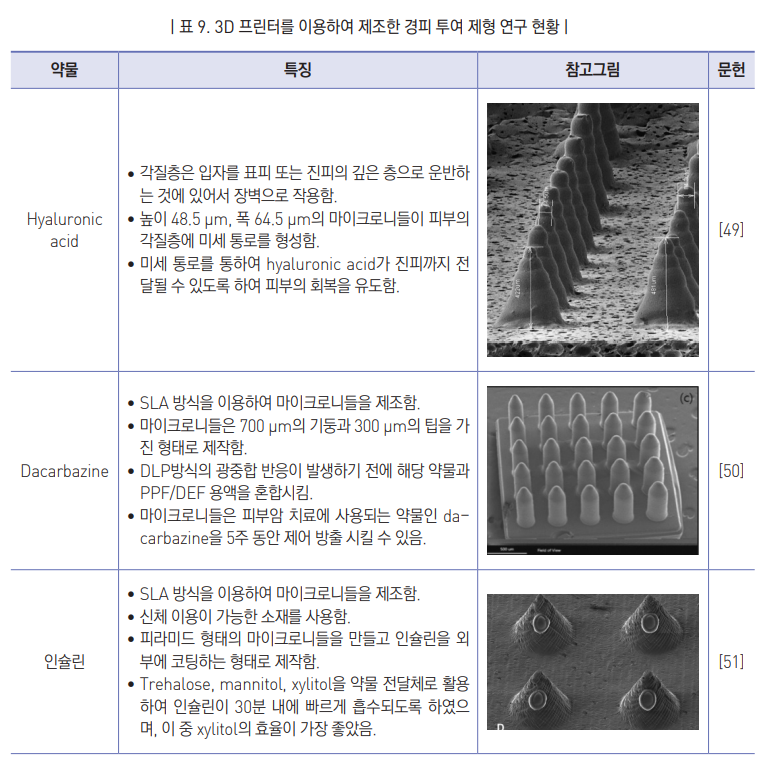
- 3D 프린터를 이용한 다양한 경피투여 시스템 중 마이크로니들 연구가 가장 활발하게 진행중임.
- 마이크로니들은 바늘의 크기가 마이크로 단위로 매우 작아서 기존에 있던 주사제형에 비해서 통증이 적고, 피부를 통해 지 속적으로 약물을 전달할 수 있으며, 환자가 스스로 투약할 수 있다는 장점을 가지고 있음.
- 특히 각질층을 통과하는 시간을 다르게 하여 약물전달 시간을 조절할 수 있으며 바늘이 각질층을 관통하여 약물을 전달하 기 때문에 적용할 수 있는 약물의 범위도 기존의 경피투과 시스템에 비해 넓어졌음.
- 기존의 마이크로니들 제조 기술의 경우, 공정상의 한계로 인해 단순한 구조의 마이크로니들로 그 형태가 제한되어있었으 최근 3D 프린팅 기술이 마이크로니들 개발에 적용되면서 기존보다 다양하고 복잡한 구조의 바늘 제조가 가능할 뿐만 아니라 약물 방출 속도를 기존보다 훨씬 다양하게 조절할 수 있게 되었음.
- 또한 3D 프린팅 기술을 기반으로 제작된 용해형 마이크로니들과 후면의 약물층에 다양한 종류의 약물을 다양한 용량으로 탑재하여 개인별 약물의 종류와 용량을 조절할 수 있는 환자 맞춤형 마이크로니들 패치 시스템 개발이 가능함.
- 현재 마이크로니틀 패치 시스템을 포함한 다양한 3D 프린팅 기술기반 경피투과 시스템의 개발연구가 진행중이며 그 사례 를 표 9에 요약하였음.

3D 프린팅 기술을 이용한 좌제 (suppository)의 제조
- 좌제는 항문 또는 질에 적용하는 고형의 외용제로 체강에서 융해·연화 혹은 용해되어 국소 또는 전신작용을 나타내는 제 형을 말함.
- 좌제는 주로 소화기관을 거치면서 약물이 불안정해지는 경우, 약물이 위점막을 자극하는 경우, 간 초회통과를 많이 받는 약물의 경우 또는 약물복용이 어렵거나 불가능한 환자에게 적용하는 경우에 유용하게 쓰임.
- 3D 프린팅 기술을 이용하여 만들어진 좌제는 개인에게 최적화될 수 있음.
- 사람마다 질이나 항문의 크기가 다르기 때문에 개인에 맞는 좌제의 사이즈가 다를 수 있으며, 3D 프린터를 이용하여 좌제 의 사이즈나 모양을 조절하면 개인 맞춤형 좌제를 제조할 수 있음.
- 그 뿐만 아니라 좌제를 인쇄하는 과정에서 좌제의 외형이나 내부구조를 변경하여 방출속도를 조절할 수 있음.
- 3D 프린팅 기술을 활용한 다양한 좌제 개발 연구 사례를 표 10에 요약하였음.


3D 프린팅 기술을 이용한 이식제 (implant)의 제조
- 이식제는 서방형 매트릭스 내에 약물을 함유한 제형으로 치료가 필요한 조직 내 혹은 주위에 삽입하여 약물을 전달함으로 서 치료효과를 높이고 전신독성의 부작용을 낮추는 제형임.
- 또한 방출제어 기술을 이용하여 장기간 동안 전신에 약물을 일정한 속도로 전달하는 목적으로도 유용하게 사용됨.
- 기존의 이식제 제조 기술은 이식제의 모양 및 정교한 내부 구조 설계에 있어서 한계가 있으며, 전달 물질과 활성 약물의 균 일 혼합물로 제조하여 방출 패턴의 조절이 어렵기 때문에 사용범위의 제약이 있음.
- 3D 프린팅 기술은 미세 구조를 작은 오차범위 내로 인쇄가 가능하기 때문에 이식제의 외형 또는 내부구조를 정교하게 변 경함에 따라 약물의 방출 패턴을 조절할 수 있음.
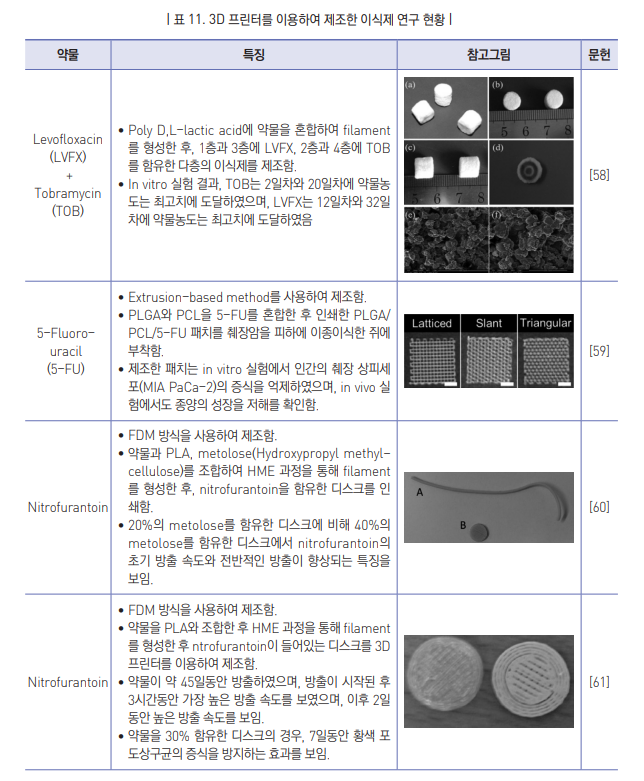
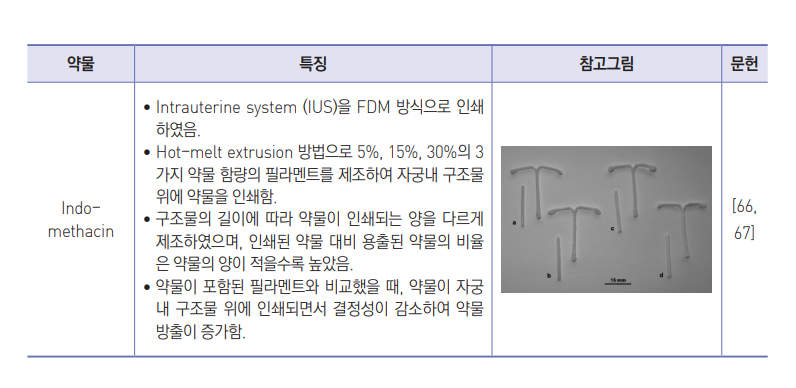
- 3D 프린팅 기술을 활용한 다양한 좌제 개발 연구 사례를 표 11에 요약하였음.

4. 3D 프린팅 의약품의 미래 방향
3D 프린팅과 맞춤의약품
3D 프린팅 기술은 소품종 대량생산에 적합한 생산기술로서 환자의 특성에 따라 다양한 종류의 의약품을 제공해야 하는 개인 맞춤형의약품의 생산에 최적화된 방식임.
환자 맞춤형 약품은 개별 환자에 따른 용량등을 조절하여 치료효과를 극대화시키고 부작용의 최소화할 수 있을 뿐만 아니라 경제적인 관점에서도 시행착오로 인해 낭비되는 많은 의료비용을 절감시킬 수 있음.
반면, 생산의 측면에서는 현재의 고형제 생산방식에 비해 효율성이 크게 떨어지기 때문에 당장 3D 기술을 이용한 경구용 고 형제의 생산은 가능할지라도 상업화는 쉽지 않은 상황이며, 이는 2015년 세계최초의 3D 프린팅 경구용 속붕해정인 Spritam의 사례를 통해서도 알 수 있음.
3D 프린팅 기술에 의한 맞춤 의약품의 개발방향은 단순히 기존의 단순한 형태의 정제를 3D 프린터로 인쇄하는 기초적인 수 준의 제형개발이 아닌 기존 제형의 단점을 극복하는 첨단 3D 프린팅 제형을 개발하는 것이 바람직함.
3D 프린팅의 경제적 측면
의료기기 영역에서 3D 프린터는 환자의 비용 절감과 부가 가치가 높은 맞춤형 기기를 생산할 수 있는 장점이 있음.
예를 들어, 보철용 팔다리가 환자에게 완벽하게 적합하면 더 편안하고 감염과 다른 합병증의 위험을 줄일 수 있음.
무릎관절 또는 엉덩이뼈를 환자맞춤형 장치로 교체하면 수술 시간과 발생되는 의료 비용을 크게 줄일 수 있을 뿐만 아니라, 심미적인 장점을 통해 신속한 치료를 촉진할 수 있음
반면, 3D 프린팅을 이용한 의약품의 낮은 생산성은 해결해야 할 과제임.
기존 제약산업에서 정제나 캡슐제를 생산하는 공정은 매우 신속하고 정확하며 저렴하게 의약품을 생산할 수 있음.
보고에 따르면 정제의 생산 단가는 생산 지역에 따라 다르지만 대략적으로 정제당 1~10원 내외인 것으로 알려져 있음 [68].
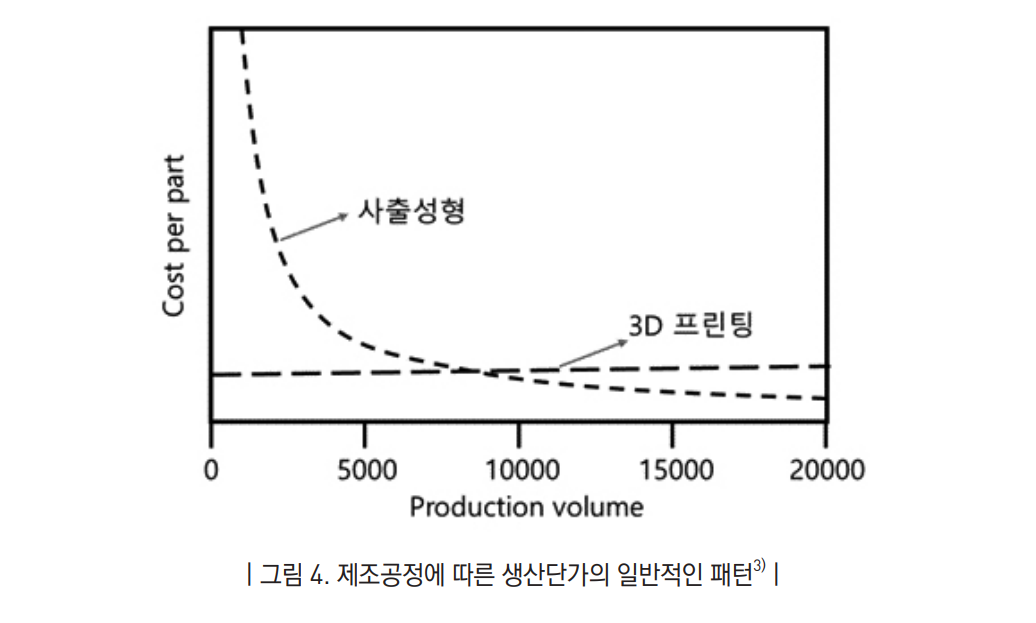
대량 생산을 통해 비용이 절감되는 조형가공방식과 다르게 3D 프린팅은 생산량이 개별 단가에 크게 영향을 주지 않음 [69].
이와 같은 제조 공정의 차이로 인해 3D 프린팅으로 기존 의약품 생산을 대체하는 것은 큰 장점이 없으며 오히려 약제비의 증 가를 가져올 수 있음.
3D 프린팅 기술의 도입을 통한 3D 의약품 상용화를 위해서는 미충족 환자맞춤형 의약품 수요에 대한 연구와 의료 비용 절감 을 충족시키기 위한 지속적인 연구가 필요함.
그럼에도 불구하고 미래에 잠재적으로 환자가 가정에서 자신의 의약품을 인쇄하며 발생하는 비용 효과 개선은 새로운 의약품 제조·유통 패러다임의 변화를 가져올 수 있고 3D 프린팅 기술을 통한 연구 초기 단계에서 시간과 비용 절감은 빠르게 변화하 는 제약산업의 발전 방향에 미래가치가 될 수 있음.
3D 프린팅 기술을 활용한 첨단제형의 제조
2015년 세계최초의 3D 프린팅 의약품이 미국 FDA의 승인을 받아 2016년 시장에 출시된 Spritam은 3D 프린팅을 통하여 특정 환자와 사용자에게 적합한 맞춤형 의약품 도입이 가능한 상징적인 의미를 가지고 있음.
비록 Spritam은 미래에 잠재적으로 환자가 가정에서 자신의 의약품을 인쇄하는 새로운 의약품 제조·유통의 패러다임 변화 가능성을 제시하였으나, 시장에서의 파급효과는 미미하였으며 현재는 생산이 중단된 상태임.
Spritam 출시 이후 현재까지 3D 프린팅 기술을 이용한 의약품의 출시는 일어나고 있지 않음.
하지만 3D 프린팅 기술은 연구 초기 단계에서 시간과 비용을 절감하여 나중에 발생할 수 있는 개발 실패에 따른 내재적 위험 을 감소시키는 새로운 제약산업 방향에 맞는 혁신적 제조 컨셉의 패러다임에 부합할 수 있을 뿐만 아니라 기존의 생산방식으 로는 생산하기 어려운 복잡한 형태의 구조물도 쉽게 인쇄할 수 있는 그 잠재적인 가능성이 충분한 미래의 생산방식임.
3D 프린팅 의약품이 시장에서 성공하기 위해서는 다품종소량생산이라는 일반적인 측면에서의 장점을 뛰어넘는 기술적으로 기존의 제제와 차별화되는 3D프린팅 제형의 개발이 필수적이며 앞으로 3D 프린팅 의약품의 개발방향 역시 기존과 차별화된 형태의 제형개발로 진행되어야 할 것임.
5. 결론 및 제언
FDA에서 최초로 허가되어 시판된 3D 프린팅 의약품이 보여준 환자맞춤형 의약품 제조의 가능성에도 불구하고 여전히 의약 품 3D 프린팅 기술이 극복해야 할 많은 난관이 존재함.
다양한 적층방식의 3D 프린팅 기술이 존재하지만 허가된 의약품 소재를 활용할 수 있는 3D 프린팅 기술은 제한되어 있고 (결 합제 분사 방식, 소재 압출 방식) 느린 3D 프린팅 의약품의 생산속도는 가격 경쟁력을 갖기 어려움.
환자맞춤형 3D 프린팅 의약품의 시장성을 가치공학적으로 분석하면 다음과 같음.
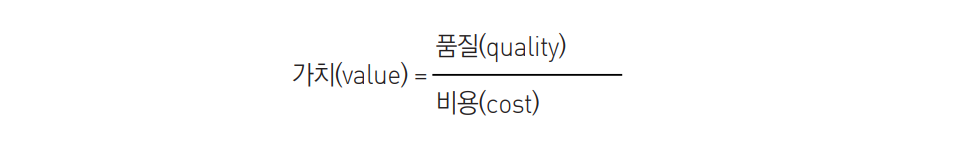
- 식에서 보는 것처럼 환자맞춤형 3D 프린팅의 시장 가치를 입증하려면 기존 의약품과 비교했을 때 비용(혹은 시간)을 줄여 주거나 품질(혹은 효과)이 월등해야 함.
- 3D 프린팅 의약품은 속도의 한계로 인해 기존 의약품에 비해 비용이 증가할 수밖에 없고 이를 상쇄하기 위해서는 환자맞 춤형 의약품을 통해서 얻게 되는 효과(품질)가 비약적으로 증가해야 그 가치를 인정받을 수 있음.
- 결국 환자맞춤형 3D 프린팅 의약품을 통해서 3D프린팅 제형의 장점을 극대화 시킬 수 있는 품목의 발굴과 기존의 제형과 는 차별화되는 새로운 가치를 갖는 제형의 개발 그리고 지속적인 비용 절감의 노력들이 환자맞춤형 3D 프린팅 의약품의 가치를 인정받을 수 있도록 할 것임.
현재 FDM 방식에 집중되어 있는 의약품 3D 프린팅 연구를 다양화하여 비교적 대량 생산이 가능하고 허가된 의약품 소재의 활용이 가능한 결합제 분사 방식의 3D 프린팅 플랫폼 기술을 확보하려는 시도가 필요하고 이를 이용한 의약품 생산 기술을 확보하려는 노력이 요구됨.
포스트 COVID-19 시대에도 유효한 키워드인 언택트(untact)와 온택트(ontact)는 이미 우리의 일상을 바꾸었고 시대의 변 화에 따라 사회 혹은 국가 단위로 표준이 변화하는 뉴노말 시대(new normal)를 우리는 맞이하게 될 것임. 언택트와 온택트 에 부합하는 혁신적인 제조공정에 기반한 3D 프린팅 의약품은 제약산업의 디지털 전환을 의미하며 한국이 가지고 있는 ICT 의 강점을 제약산업에 융합시키는 강력한 플랫폼 기술로 성장할 수 있음. 3D 프린팅 의약품은 포스트 코로나 시대에 변화하 는 제약산업의 패러다임을 대표하는 혁신적인 디지털 제조 컨셉임.
3D 프린팅 의약품이 글로벌 경쟁력을 가진 플랫폼 기술로 성장하기 위해서는, 3D 프린팅 의약품 상용화를 위한 학계와 산업 계의 통합적이며 다각적인 연구개발을 통한 기존 생산방식 제형의 한계를 뛰어 넘어 3D 프린팅 기술의 장점을 살릴 수 있는 제형으로의 개발이 절대적으로 필요하고, 의약품 제조·유통 시스템이나 약가 제도에 대한 국가 차원의 정책적, 제도적인 변 화가 뒷받침 되어야 함.
출저 : keit pd 이슈리포트
'사회경제' 카테고리의 다른 글
| 자율주행기술 활용 상용차 위험환경 극복 기술 동향 (0) | 2023.02.26 |
|---|---|
| 탄소소재 적용 전자파 차폐 산업현황과 기술전망 (0) | 2023.02.25 |
| 비대면 휴먼케어 서비스 로봇 기술 현황 및 발전 방향 (0) | 2023.02.24 |
| 전기자동차 배터리 팩 고밀도화 기술 (0) | 2023.02.24 |
| 항공용 금속소재 자립화 현황 및 전망 (0) | 2023.02.22 |




댓글